TRAITER LA PERTE DE VISION GRÂCE À LA THÉRAPIE GÉNIQUE
Parmi les traitements novateurs contre les maladies oculaires, aucun n’a reçu autant d’attention que la thérapie génique. Et à juste titre. La toute première thérapie génique, LuxturnaMD, a été approuvée aux États-Unis en 2017 afin de traiter les personnes porteuses de mutations sur le gène RPE65 qui causent l’amaurose congénitale de Leber ou la rétinite pigmentaire. Des dizaines de thérapies géniques font actuellement l’objet d’essais cliniques, et bien d’autres sont à l’étape de la recherche et du développement. Vous découvrirez ci-dessous les différents types de thérapie génique, à qui elles peuvent convenir, ainsi qu’une liste des essais cliniques en cours.
QU’EST-CE QUE LA THÉRAPIE GÉNIQUE ET COMMENT FONCTIONNE-T-ELLE?
Chaque cellule du corps à sa fonction propre. Les cellules pulmonaires absorbent l’oxygène, les cellules musculaires nous aident à bouger, les cellules rétiniennes captent et transmettent la lumière pour former des images, et ainsi de suite. Mais comment font-elles pour savoir ce qu’elles doivent faire? La réponse se trouve dans nos gènes. Composés d’ADN, les gènes sont le manuel d’instruction des cellules. Ils leur dictent quelles molécules produire et comment se comporter.
La thérapie génique a pour objet de modifier le comportement d’une cellule en créant un nouveau gène ou en remplaçant un gène défectueux. Elle est à l’avant-plan des nouveaux traitements pour les maladies héréditaires de la rétine (MHR), comme la rétinite pigmentaire ou la maladie de Stargardt, qui sont causées par un gène défectueux ou porteur d’une mutation. Des chercheurs étudient par ailleurs son potentiel contre d’autres maladies menant à une perte de vision, notamment la dégénérescence maculaire liée à l’âge (DMLA), l’œdème maculaire diabétique (OMD) et les maladies cornéennes. Voici donc les types de thérapie génique les plus courants :
REMPLACEMENT DE GÈNES
Comme son nom l’indique, le remplacement de gènes consiste à introduire un nouveau gène pour en remplacer un autre défectueux. Ce traitement, à la base de Luxturna, la toute première thérapie génique approuvée, est utilisé pour de nombreuses MHR. Il peut être une option tout indiquée pour les personnes qui connaissent leur mutation.
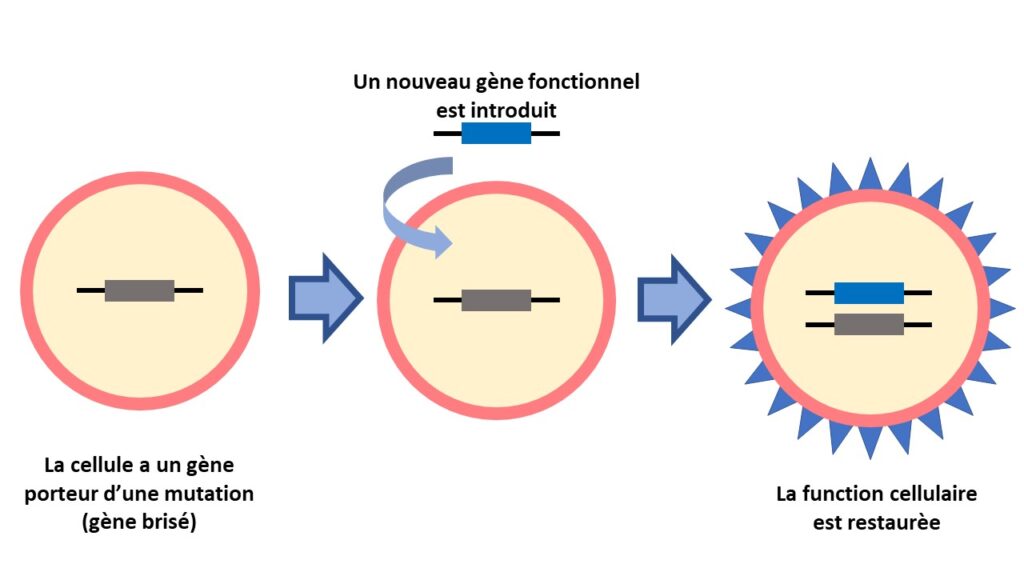
MODIFICATION DU GÉNOME
La modification du génome est aussi un traitement qui cible un gène particulier. La mutation génétique doit donc être connue. Des ciseaux moléculaires sont utilisés pour retirer la mutation et ainsi « modifier » le gène. Ce traitement est à l’étude pour les MHR comme la rétinite pigmentaire, l’amaurose congénitale de Leber et le syndrome d’Usher.
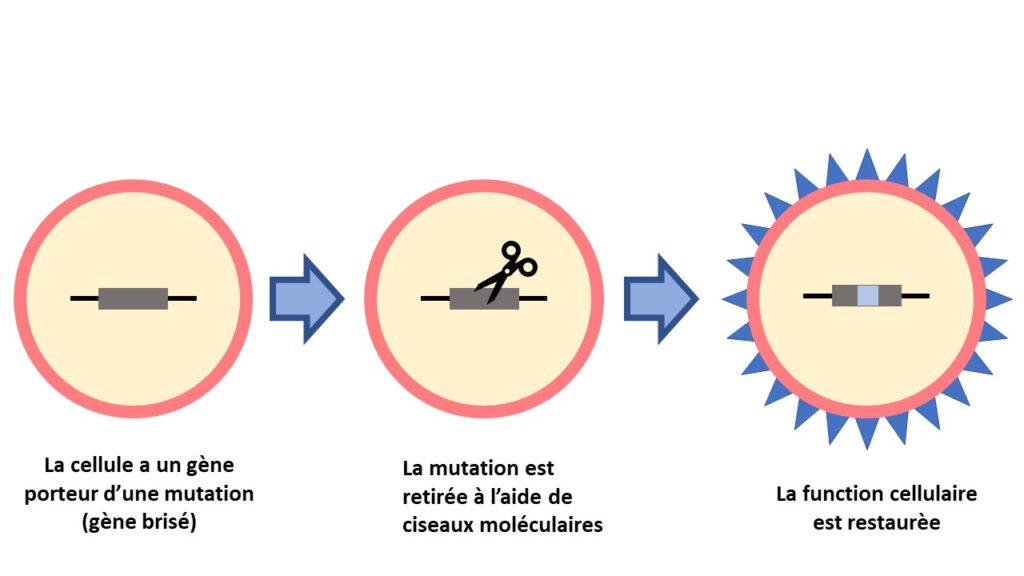
THÉRAPIE CONTRE LA MORT CELLULAIRE
Les maladies de la rétine telles que les MHR, la DMLA et l’OMD ont des causes génétiques et environnementales diverses, mais toutes ont une issue similaire : les cellules rétiniennes qui captent et transmettent la lumière finissent par mourir, menant à une perte de vision. Des chercheurs ont mis au point des thérapies dites « neuroprotectrices ». Des gènes sont introduits dans les cellules de la rétine pour les préserver. Cette thérapie, contrairement aux deux précédentes, ne vise pas de gène particulier; un seul traitement pourrait donc être utilisé pour les MHR causées par diverses mutations, les MHR dont la mutation est inconnue ou les maladies, comme la DMLA, qui n’ont pas de cause génétique.
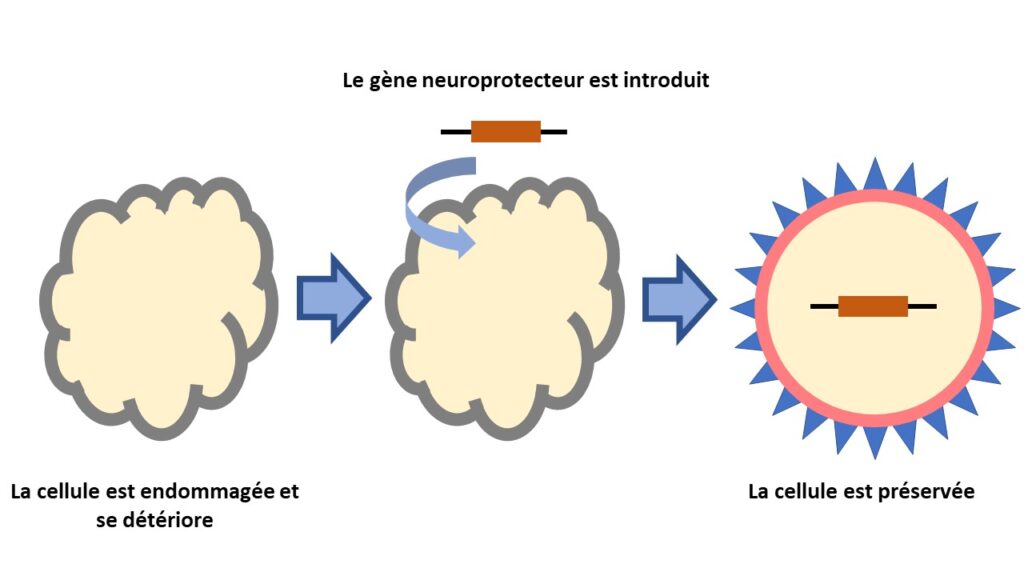
THÉRAPIE GÉNIQUE POUR REMPLACER LES INJECTIONS ANTI-VEGF
Les injections anti-VEGF sont le traitement le plus courant contre la DMLA et l’OMD. Ces maladies sont caractérisées par une croissance incontrôlée des vaisseaux sanguins dans la rétine et une fuite de liquide dans l’œil, ce qui entraîne la perte de vision. Les anti-VEGF ralentissent la croissance des vaisseaux sanguins. Des essais cliniques ont lieu pour déterminer s’il est possible d’introduire dans les cellules rétiniennes des gènes qui leur donneront l’ordre de produire leur propre anti-VEGF. Autrement dit, les chercheurs essaient de les transformer en « usines anti-VEGF » dans le but de réduire la fréquence des injections.
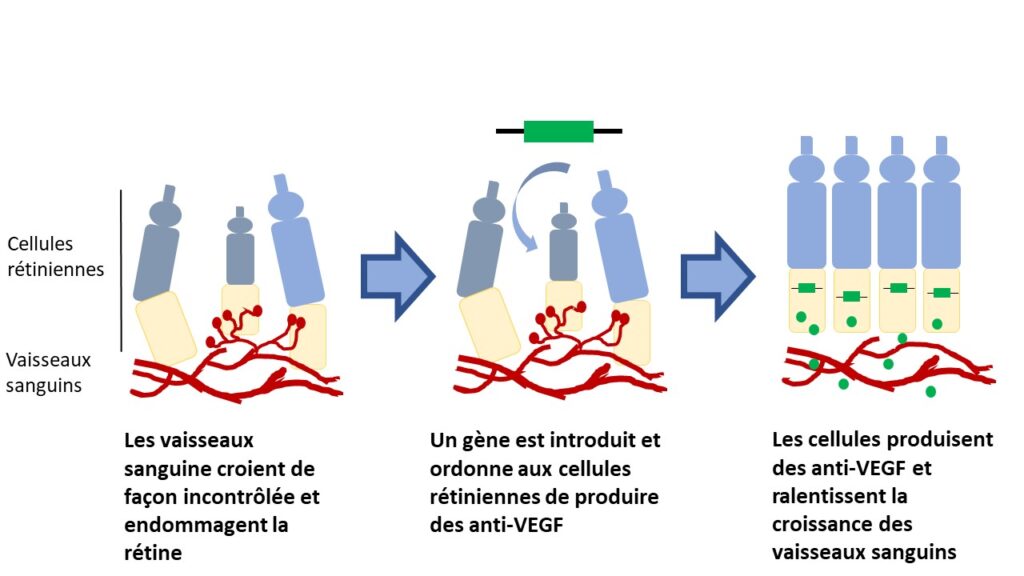
DES OBSTACLES MALGRÉ TOUT
Bien que prometteuse, la thérapie génique génère son lot d’obstacles et de considérations importantes que doivent peser les patients. À l’heure actuelle, les thérapies les plus intéressantes ciblent un gène particulier ou s’attaquent aux MHR comme la rétinite pigmentaire ou l’amaurose congénitale de Leber.
Mettre au point une thérapie génique pour chaque gène ou mutation est un travail qui demande beaucoup de temps et d’argent, et ces thérapies ne fonctionnent que pour les personnes ayant exactement la mutation génétique visée.
Le stade de la maladie est aussi un enjeu. La thérapie génique n’est efficace que s’il reste assez de cellules rétiniennes saines dans lesquelles faire l’intervention. Si les cellules saines se font rares, les traitements à base de cellules souches ou la rétine artificielle pourraient mieux convenir.
LUXTURNA : LA PREMIÈRE THÉRAPIE GÉNIQUE CONTRE LES MHR
Luxturna est le premier traitement contre les MHR approuvé aux États-Unis, en Europe et, espérons-le, bientôt au Canada. Il s’agit d’une thérapie génique s’adressant aux personnes atteintes de la rétinite pigmentaire ou de l’amaurose congénitale de Leber et qui présentent une mutation sur les deux copies du gène RPE65. Elle ne guérit pas ces maladies, mais peut améliorer la vue des patients et ralentir leur perte de vision.
ESSAIS CLINIQUES
De nombreuses thérapies géniques font l’objet de recherches pour traiter différents types de perte de vision, et beaucoup sont testées sur des patients dans le cadre d’essais cliniques. Vous trouverez ci-dessous une liste de certains essais ayant lieu partout dans le monde. Chaque essai a ses propres critères d’admissibilité. Si vous souhaitez participer à un essai clinique, parlez-en d’abord à votre professionnel de la vue.
Peut-être aimeriez-vous aussi participer à une étude sur l’histoire naturelle. Ces études permettent de recueillir des données importantes sur une maladie, en particulier les maladies rares, et ainsi d’orienter la conception des essais cliniques.
Pour en savoir plus sur les essais cliniques, contacter notre ligne d’information sur la santé au 1 888 626-2995 ou au healthinfo@fightingblindness.ca.
ACHROMATOPSIE
| Gène | Responsable de l’essai | Phase | Région |
|---|---|---|---|
| CNGA3/CNGB3 | MeiraGTx | 1/2 | Royaume-Uni |
| CNGA3 | University Hospital Tuebingen | 1/2 | Allemagne |
| CNGA3 | MeiraGTx/Janssen | 1/2 | États-Unis, Royaume-Uni |
| CNGB3 | AGTC/National Eye Institute (NEI) | 1/2 | États-Unis |
| CNGA3 | AGTC | 1/2 | États-Unis, Israël |
CHOROÏDÉRÉMIE
| Gène | Responsable de l’essai | Phase | Région |
|---|---|---|---|
| REP1 | NightstarX/Biogen | 3 | Canada (Montréal et Vancouver), États-Unis, Europe, Royaume-Uni |
| REP1 | University Hospital Tuebingen | 2 | Allemagne |
| REP1 | Spark Therapeutics | 1 | États-Unis |
| REP1 | University of Oxford | 1/2 | États-Unis |
| REP1 | 4D Molecular Therapeutics, Roche Pharmaceuticals | 1/2 | États-Unis, Israël |
AMAUROSE CONGÉNITALE DE LEBER
| Gène | Responsable de l’essai | Phase | Région |
|---|---|---|---|
| CEP290 | ProQR [QR-110 (Sepofarsen)] | 2/3 | Canada (Montréal et Vancouver), États-Unis, Europe, Royaume-Uni |
| CEP290 | Allergan [AGN-151587] | 1/2 | États-Unis |
| GUCY2D | Atsena Therapeutics Inc. [SAR439483] | 1/2 | États-Unis |
| RPE65 | MeiraGTX | 1/2 | Royaume-Uni |
NEUROPATHIE OPTIQUE HÉRÉDITAIRE DE LEBER
| Gène | Responsable de l’essai | Phase | Région |
|---|---|---|---|
| G11778A | National Eye Institute (NEI) | 1 | États-Unis |
| G11778A ND4 | Gensight Biologics | 3 | États-Unis, Royaume-Uni, Taïwan |
RÉTINOSCHISIS
| Gène | Responsable de l’essai | Phase | Région |
|---|---|---|---|
| RS1 | AGTC [rAAV-hRS1] | 1/2 | États-Unis |
| RS1 | NEI | 1/2 | États-Unis |
RÉTINITE PIGMENTAIRE
| Gène | Responsable de l’essai | Phase | Région |
|---|---|---|---|
| PDE6B | Horama | 1/2 | Europe |
| RHO | ProQR [QR-1123] | 1/2 | États-Unis |
| RPE65 | MeiraGTX [OPTIRPE65] | 1/2 | États-Unis |
| USH2A | ProQR [QR-421a] | 1/2 | Canada (Montréal), États-Unis, Europe |
| RLBP1 | Novartis [CPK850] | 1/2 | Europe |
SYNDROME D’USHER
| Gène | Responsable de l’essai | Phase | Région |
|---|---|---|---|
| MYO7A | Sanofi [SAR421869] | 1/2 | États-Unis, Europe |
| USH2A | ProQR [QR-421a] | 1/2 | Canada (Montréal), États-Unis, Europe |
RÉTINITE PIGMENTAIRE LIÉE À L’X
| Gène | Responsable de l’essai | Phase | Région |
|---|---|---|---|
| RPGR | AGTC | 1/2 | États-Unis |
| RPGR | MeiraGTX | 1/2 | États-Unis, Royaume-Uni |
| RPGR | NightstarX/Biogen | 2/3 | États-Unis, Royaume-Uni |
| RPGR | 4D Molecular Therapeutics | 1/2 | États-Unis |
DÉGÉNÉRESCENCE MACULAIRE LIÉE À L’ÂGE
| Responsable de l’essai | Phase | Région |
|---|---|---|
| Regenxbio [RGX-314] | 2 | États-Unis |
| Hemera/Janssen [AAVCAGsCD59] | 1 | États-Unis |
| Hemera/Janssen [AAVCAGsCD59] | 2 | États-Unis |
| Adverum [ADVM-022] | 1 | États-Unis |
| Adverum [ADVM-022] | 2 | États-Unis |
Ces tableaux ont été mis à jour en décembre 2020.
Cette page fait partie de la série « Essais cliniques » de Vaincre la cécité Canada.
Pour en savoir plus sur les essais cliniques, vous pouvez consulter le site clinicaltrials.gov. Il s’agit d’un bon point de départ de votre démarche, mais l’information n’y est pas toujours exhaustive et de nombreux essais figurant sur le site n’ont pas été approuvés par la FDA (Food and Drug Administration des États-Unis) et pourraient ne pas répondre aux normes de sécurité de base. Consultez toujours votre professionnel de la vue avant de participer à un essai clinique.
EN SAVOIR PLUS
- Discussion sur la génétique des maladies héréditaires de la rétine avec le Dr Rob Koenekoop : Dans cet article, le Dr Rob Koenekoop explique comment ses travaux sur les MHR ont conduit à de nouveaux traitements et quel rôle les patients peuvent jouer dans cette recherche. [Accessible en anglais seulement]
Unissons nos forces
Découvrez comment votre soutien peut contribuer à tracer un avenir sans cécité! Soyez informé en exclusivité des dernières percées de la recherche en santé de la vision et des événements dans votre région en vous abonnant à notre infolettre.

